プレスリリース配信元:国立大学法人千葉大学
千葉大学大学院医学研究院 平原 潔教授と横浜市立大学大学院医学研究科 金子 猛教授、柳生 洋行助教(研究当時:千葉大学大学院医学薬学府 特別研究学生)らの研究グループは、アレルギー性炎症を悪化させる「病原性Th2(ティーエイチツー)細胞」 (注1)が、免疫細胞が持つ「脂肪滴を分解して再利用する仕組み」によって誘導されることを明らかにしました。今後、脂肪分解経路を標的とした新たなアレルギー疾患の治療法の開発が期待されます。
本研究成果は、2025年10月24日に、国際科学誌Science Immunology に公開されます。
■研究の背景
私たちの体を守る免疫には、ウイルスや細菌などの病原体を排除する「1型免疫」と、ダニや花粉などに反応する「2型免疫」があります。この2型免疫を司っているのが「Th2細胞」です。一方で、喘息などのアレルギー疾患の患者では、病気が悪化する原因となる「病原性Th2細胞」が体の中に出現しますが、その誘導機構は不明でした。
近年、免疫細胞が、生体内でどのように栄養素(脂肪や糖)を使うかによって、その細胞の性質や働き方が変わる「免疫代謝」という仕組みの重要性が明らかになってきました。しかし、病原性Th2細胞の誘導に「免疫代謝」がどのように関わっているのかはこれまで不明でした。
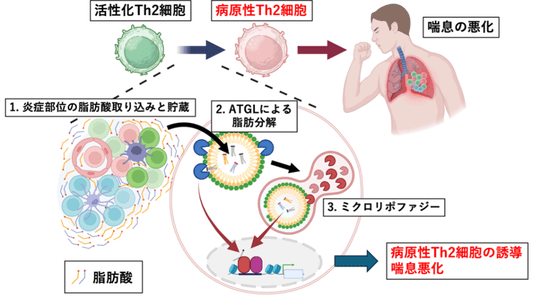
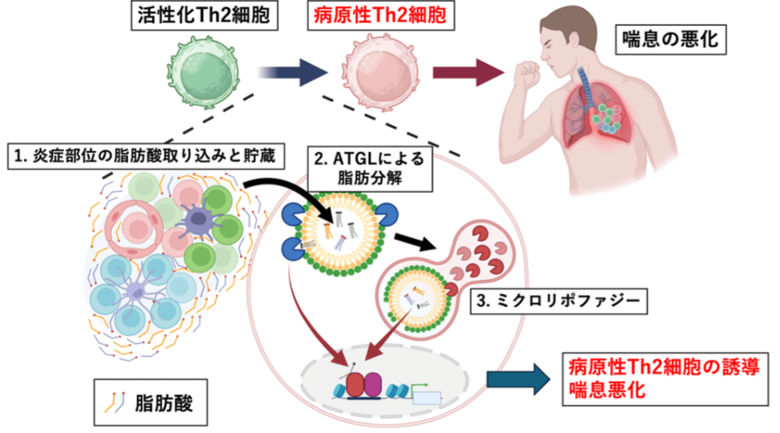
図:脂肪分解経路が病原性Th2細胞を誘導する
■研究のポイント
私たちの今回の研究の結果、抗原刺激で活性化したTh2細胞が、炎症組織で増加する特定の脂肪酸を「脂肪滴」として細胞内に燃料として蓄えること、その「脂肪滴」を脂肪分解酵素やオートファジー(注2)機構によって少しずつ分解(燃焼)することで、病原性Th2細胞が誘導されることを突き止めました。
1. 喘息モデルマウスの炎症部位では、オレイン酸などの「脂肪酸」が顕著に増加していた(図中1)。
2. その脂肪酸を、活性化したTh2細胞が取り込んで「脂肪滴」に一時的に蓄積し、脂肪分解酵素ATGL (注3)(図中2)や「ミクロリポファジー」 (注4)と呼ばれる特殊なオートファジー機構(図中3)によって脂肪滴を分解することで、病原性Th2細胞が誘導された。
3. 脂肪分解酵素ATGLを欠損させたマウスでは、ミクロリポファジーの抑制、病原性Th2細胞の減少とともに、喘息の主症状である好酸球性気道炎症の改善も確認した。
4. 好酸球性副鼻腔炎患者においても脂肪分解経路を介した病原性Th2細胞誘導機構が同様に働いていることを確認し、難治性の病態との関連を示した。
■今後の展望
本研究では、炎症が生じている組織で免疫細胞が特定の脂肪酸を取り込んで「燃料」として蓄え、それを少しずつ分解(燃焼)することで、自ら喘息などの症状を悪化させる細胞に変貌するというメカニズムを解明しました。この脂肪分解経路を標的として、脂肪分解酵素ATGLやミクロリポファジーの働きを適切に制御する治療法を開発することを目指しています。この取り組みが、既存のステロイド治療や生物学的製剤では十分に抑えられなかった喘息や好酸球性副鼻腔炎などの難治性アレルギー疾患に苦しむ患者の、治療の選択肢を広げる一歩になることを願っています。
■用語解説
注1)病原性Th2細胞:Th2細胞は、免疫の司令塔となるヘルパーT細胞の一種で、特に寄生虫に対する感染から体を守る。一方で、アレルゲン(ダニや花粉など)に対しても反応し、炎症を引き起こす物質(サイトカイン)を分泌する。このTh2細胞の中でも一部の集団が病原性Th2細胞となる。病原性Th2細胞は、アレルゲンを記憶して炎症組織に長くとどまり、再びアレルゲンを感知すると多量のサイトカインを分泌し、通常のTh2細胞よりも強い炎症を引き起こす。喘息などのアレルギー疾患の慢性化や難治化に関与する。
注2)オートファジー:細胞内部の異常なタンパク質や不要になったタンパク質、細胞小器官をリソソーム(細胞内の分解装置)で分解・再利用する仕組みで、「自食作用」とも呼ばれる。細胞を正常な状態に保つための重要な維持管理機能。
注3)ATGL:脂肪滴の内に貯蔵された中性脂肪(トリグリセリド)を分解する酵素で、細胞が脂肪をエネルギー源として利用する際に中心的な役割を果たす。
注4)ミクロリポファジー:脂肪滴を分解する特殊なオートファジーで、細胞内の分解装置であるリソソームが脂肪滴を直接取り込んで分解する現象を指す。
■論文情報
タイトル:Lipolysis-microlipophagy cascade regulated by adipose triglyceride lipase drives pathogenic adaptive type 2 immunity
著者:Hiroyuki Yagyu, Masahiro Kiuchi, Atsushi Sasaki, Eisuke Itakura, Kota Kokubo, Chiaki Iwamura, Atsushi Onodera, Ami Aoki, Takahisa Hishiya, Kaori Tsuji, Takuto Hiramoto, Rie Shinmi, Yuri Sonobe, Takahiro Arano, Kanae Ohishi, Shigenori Baba, Junya Kurita, Tomohisa Iinuma, Syuji Yonekura, Yu Hara, Motoko Yagi Kimura, Shinichiro Motohashi, Damon J Tumes, Toyoyuki Hanazawa, Takeshi Kaneko, Toshinori Nakayama, Kiyoshi Hirahara
雑誌名:Science Immunology, 24 Oct 2025
DOI:10.1126/sciimmunol.adp0849
■研究プロジェクトについて(研究経費)
本研究は、以下の支援を受けて実施しました。
日本学術振興会(JSPS) 科学研究費助成事業(科研費):基盤研究(S)(課題番号:JP19H05650)、基盤研究(B)(課題番号:JP23K27607)、若手研究(課題番号:JP22K15485)、学術変革領域研究(B)(課題番号:JP21H05120、JP21H05121)
日本医療研究開発機構(AMED):免疫アレルギー疾患実用化研究事業「生体内における病原性Th2細胞誘導機構解明による難治性アレルギー性疾患の治療法開発」、「生体内における病原性Th2細胞の組織常在性獲得機構解明による難治性アレルギー性疾患の治療法開発」、革新的先端研究開発支援事業「気道組織における病的リモデリング(線維化)機構の解明と病態制御治療戦略の基盤構築」、「外部環境刺激による組織炎症記憶形成機構の解明と難治性アレルギー性疾患の病態制御治療戦略の基盤構築」、AMED SCARDAワクチン開発のための世界トップレベル研究開発拠点の形成事業「千葉シナジーキャンパス(千葉大学 未来粘膜ワクチン研究開発シナジー拠点) 」、革新的先端研究開発支援事業インキュベートタイプ「三次リンパ組織を標的とした腎臓病治療法および診断法の開発」
科学技術振興機構(JST) 創発的研究支援事業「肺における組織炎症記憶の4次元制御機構の統合的解明」(課題番号:JPMJFR200R)
企業プレスリリース詳細へ
PR TIMESトップへ
データ提供 PR TIMES
本記事の内容に関するお問い合わせ、または掲載についてのお問い合わせは株式会社 PR TIMES (release_fujitv@prtimes.co.jp)までご連絡ください。また、製品・サービスなどに関するお問い合わせに関しましては、それぞれの発表企業・団体にご連絡ください。