プレスリリース配信元:国立大学法人千葉大学
千葉大学大学院医学研究院 伊藤薫教授(理化学研究所生命医科学研究センター チームディレクター)、理化学研究所生命医科学研究センター 円山信之リサーチアソシエイト(研究当時)、九州大学大学院医学研究院 二宮利治教授、東京大学大学院医学系研究科 小室一成特任教授(国際医療福祉大学大学院教授)、東京大学医科学研究所附属ヒトゲノム解析センターシークエンス技術開発分野の松田浩一特任教授(同大学大学院新領域創成科学研究科メディカル情報生命専攻クリニカルシークエンス分野教授)らの研究グループは、日本人集団と欧州人集団の心不全患者を対象に、心不全のタイプ別に異なる遺伝的な特徴を解明し、心不全が起こるメカニズムに集団ごとの違いがあることを明らかにしました。加えて、解析の結果から構築された心不全のなりやすさを点数化した「多遺伝子リスクスコア」や、心筋症の原因遺伝子である「TTN」変異のバイオマーカーを調べることで、心不全の進み方や予後を推定することが可能であることを発見しました。この成果は、心不全の精密な診断や治療薬開発につながることが期待されます。
本研究成果は、科学誌 Nature Communications にて2025年11月3日にオンライン公開されました。
■研究の背景
心不全は高齢化の進行とともに患者数が年々増え、命に関わる重大な疾患として社会的な問題となっています。これまでの大規模な遺伝子研究(ゲノムワイド関連解析:GWAS(注1))は欧米人のデータが中心であり、日本人を含む東アジアの人に特有の遺伝的要因は十分に解明されていませんでした。また、心不全には大きく分けて、狭心症や心筋梗塞などの虚血性心疾患でおきる虚血性心不全(心不全全体の47%程度)、虚血性でない心不全(心不全全体の50%以下)があります。さらに心不全には心臓の収縮機能が低下した「収縮能低下型心不全(HFrEF)」(虚血性でない心不全の37%程度)と、心臓は収縮できるものの拡張がうまくいかない「収縮能保持型心不全(HFpEF)」(虚血性でない心不全の45%程度)など複数のタイプがあり、それぞれ原因や治療の反応が異なることも問題です。
このような背景から、日本人に特有の心不全の遺伝的背景および各サブタイプの違いを理解することは、個別化医療や予防に向けて大きな意義があります。
■研究の成果
本研究ではバイオバンク・ジャパンに登録された日本人集団を対象に、心不全およびそのサブタイプ(HFrEF、HFpEF、虚血性でない心不全など)についてGWASを実施しました。分析には、全ての原因を考慮した心不全患者1万6,251例、HFrEF患者4,254例、HFpEF患者7,154例、非虚血性心不全 (NIHF) 患者1万1,122例、コントロール群として19万7577例が用いられました。
主な成果は以下の通りです。
・ 日本人集団に特有の新しい心不全関連遺伝子座(注2)(5カ所)を発見し、さらに国際共同解析や複数疾患データを組み合わせることで合計19カ所の新規遺伝子座を同定しました。
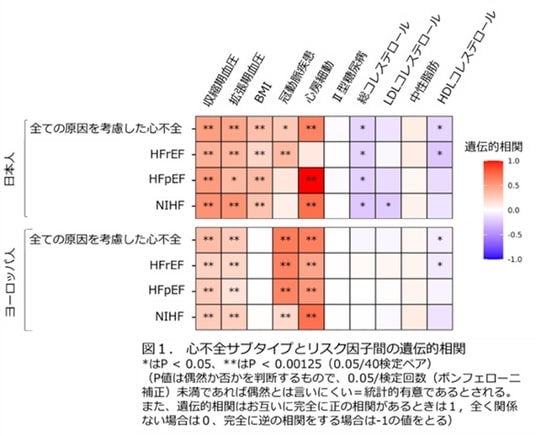
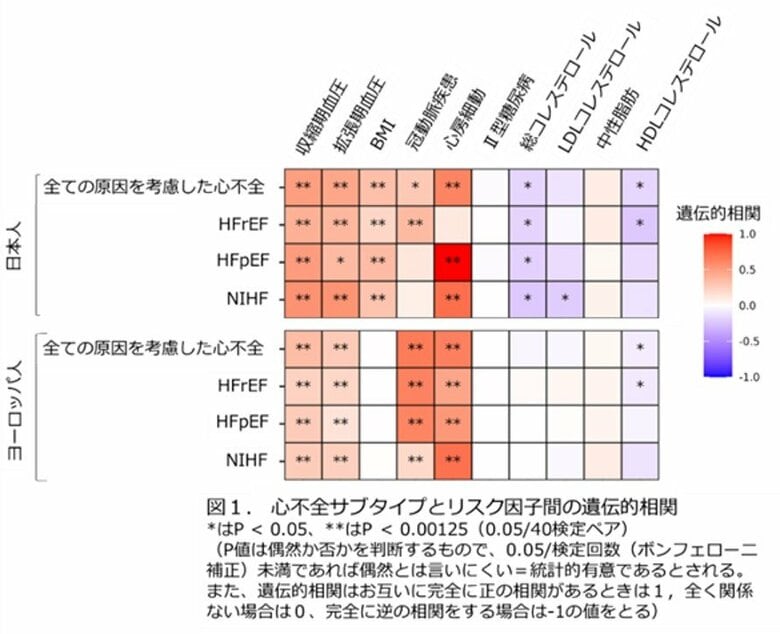
・ 遺伝的な関連を比較したところ、欧州人集団と日本人集団で違いがあることが明らかになりました。例えば、肥満度(BMI)は日本人集団でのみ心不全と関連していました。これは、東アジアの集団が比較的低いBMIでも内臓脂肪が多く、心臓への負担が大きくなりやすいためと考えられます(図1)。また全ての原因を考慮した心不全では細胞周期や老化、HFrEFはサルコメア(注3)関連、虚血性でない心不全は心臓の発生・発達などの生体内での機能的な分子経路が強調されました。
・ 心筋細胞や心筋疾患に関連する遺伝子(TTN、NEBL など)の一般的な変異が、心不全に関係していることが判明しました。
・ 特に東アジアの人に多いTTN遺伝子の変異は、日本人集団と欧州人集団で効果の大きさが異なり、心不全重症化や死亡率上昇と関係することが判明しました。この様な変異は、従来の稀な遺伝子変異を対象とした検査では見逃される可能性があり、新しい予測に役立つマーカーとなることが期待されます。
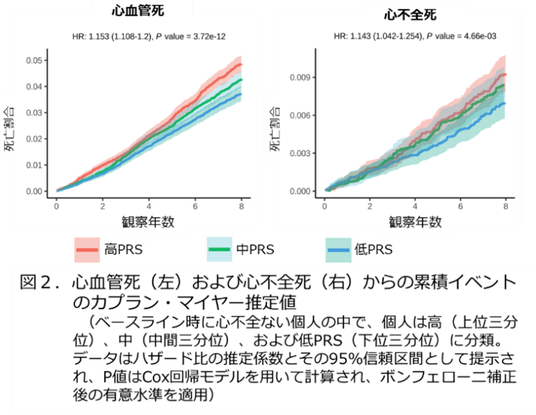
・ さらに研究グループは、心不全発症や死亡リスクを予測する「多遺伝子リスクスコア(PRS)(注4)」を独自に開発しました。日本人集団に最適化されたこのスコアは高い精度を示し、高リスク者の早期発見や死亡リスクの層別化が可能となりました(図2)。PRSが高い人は、若くして心不全を発症するリスクが高く、さらに診断時にはまだ心不全でない人でも、将来的な死亡リスクが高いことが分かりました。
■今後の展望
今回の研究は、日本人集団における心不全の遺伝的特徴と臨床への応用可能性を世界で初めて体系的に示したものです。今後はこの成果を活かし、以下の展開が期待されます。
・ 新たに発見された遺伝子や変異を手がかりにした創薬や、既存薬の有害作用予測など、より効果的かつ安全な治療法の開発。
・ 「多遺伝子リスクスコア(PRS)」の実用化により、心不全の発症リスクが高い人を早期に抽出し、個別化された生活指導やフォローアップ検診への応用。
・ さまざまな集団への知見の拡大や、それに合わせた予防・治療プランの最適化。
本成果は今後、日本発の心不全対策や精密医療構築の基盤となることが大いに期待されます。
■用語解説
注1)ゲノムワイド関連解析(GWAS:Genome-wide Association Study):多くの人の全ゲノム情報を比較し、疾患や体質に関係する遺伝的変化(多型)を網羅的に探す研究手法。集めた遺伝情報を患者群と非患者群(コントロール群)で統計解析し、病気の原因やリスクに関係する遺伝子を特定することで、個別化医療や新規治療法の開発にも活用できる。
注2)遺伝子座:「遺伝子の住所」のようなものを表す用語で、特定の遺伝子や遺伝子マーカーが染色体上のどの場所にあるかを示している。ひとつの遺伝子座には対立遺伝子(アレル)が存在しうるため、遺伝的多様性の源となる。
注3)サルコメア:心臓の拍動に不可欠な「筋収縮の最小単位」であり、アクチンとミオシンなど複数のたんぱく質線維から構成されている。サルコメアの異常は、心筋症などの心臓病の原因となることがある。
注4)多遺伝子リスクスコア(PRS:Polygenic Risk Score):病気や体質に関係する多数の遺伝子変異の効果を統合して個人ごとのリスクを数値化する指標。GWAS研究で見つかった各変異の影響度を加味して合計し、疾患のなりやすさなどを統計的に評価する。これにより個別化医療や早期予防が可能となる。
■論文情報
タイトル:Genome-wide analysis of heart failure yields insights into disease heterogeneity and enables prognostic prediction in the Japanese population
著者:Nobuyuki Enzan, Kazuo Miyazawa, Satoshi Koyama, Ryo Kurosawa, Hirotaka Ieki, Hiroki Yoshida, Fumie Takechi, Masashi Fukuyama, Ryosuke Osako, Kohei Tomizuka, Xiaoxi Liu, Kouichi Ozaki, Yoshihiro Onouchi, the BioBank Japan Project, Koichi Matsuda, Yukihide Momozawa, Hiroyuki Aburatani, Yoichiro Kamatani, Takanori Yamaguchi, Hiroshi Akazawa, Koichi Node, Patrick T. Ellinor, Michael G. Levin, Scott M. Damrauer, Benjamin F. Voight, Jacob Joseph, Yan V. Sun, Chikashi Terao, Toshiharu Ninomiya, Issei Komuro and Kaoru Ito
雑誌名:Nature Communications
DOI:10.1038/s41467-025-64659-6
■研究プロジェクトについて
本研究は、日本医療研究開発機構(AMED)の革新的先端研究開発支援事業(PRIME)「性差・個人差の機構解明と予測技術の創出」研究開発領域における研究開発課題「静的・動的オミクス融合が駆動する循環器多因子疾患システムの解明と先制医療の実現」の支援により行われました。
企業プレスリリース詳細へ
PR TIMESトップへ
データ提供 PR TIMES
本記事の内容に関するお問い合わせ、または掲載についてのお問い合わせは株式会社 PR TIMES (release_fujitv@prtimes.co.jp)までご連絡ください。また、製品・サービスなどに関するお問い合わせに関しましては、それぞれの発表企業・団体にご連絡ください。