プレスリリース配信元:千葉工業大学
---分子標的薬やバイオセンサ開発に向けた核酸材料設計の分子基盤を確立---
学校法人千葉工業大学 先進工学部生命科学科 坂本泰一教授、日本大学工学部 山岸賢司准教授(現 千葉工業大学教授)、京都大学エネルギー理工学研究所 永田崇准教授、片平正人教授、阪本知樹博士(現 東京薬科大学助教)、北海道医療大学歯学部 堀内正隆教授、鹿児島大学工学部 石川岳志教授らの共同研究により、分子標的薬やバイオセンサの材料となる核酸アプタマー 注1)について、RNAとDNAを組み合わせることで、アプタマーの柔らかさを変え、標的タンパク質へのフィットの仕方を変えられることを明らかにしました。
現在、核酸アプタマーは、抗体に代わる分子認識材料として、分子標的薬やバイオセンサ(図1)に応用されています。核酸アプタマーは、一般にDNAあるいはRNAから、SELEX法 注2)とよばれる技術によってつくられますが、今回、RNAとDNAからなるキメラアプタマーと標的タンパク質の相互作用を詳細に解析したところ、RNAとDNAの柔らかさの違いが分子認識に大きく影響していることを明らかにしました。今後、RNAとDNAを組み合わせることでアプタマーの「ゆらぎ」や標的タンパク質へのフィットの仕方を調整し、アプタマー医薬品やアプタマーセンサの設計に活用できると期待されます。
この研究の詳細は、米国化学会が発行する学術雑誌ACS Chemical Biologyに4月17日付けで掲載されました。
<研究概要>
アプタマーは、標的分子を高い特異性で認識して結合する核酸分子です。この性質を利用して、病気に関わるタンパク質を標的とする分子標的薬や、血液・唾液中のタンパク質、低分子化合物、環境汚染物質などを検出するバイオセンサへの応用が進められています。抗体の製造には細胞培養が必要ですが、核酸は化学合成できるため、製造や品質管理の面で利点があります。また、核酸は熱や乾燥に比較的強いことから、さまざまな環境で用いるバイオセンサの材料としても有望です。
通常、RNAを構成成分とするRNAアプタマー、あるいはDNAを構成成分とするDNAアプタマーが開発されています。一方で、RNAとDNAを組み合わせたキメラアプタマーにおいて、RNAとDNAの違いが標的認識にどのように影響するかは十分には明らかになっていませんでした。今回、RNAの一部をDNAに置換したキメラアプタマーと標的タンパク質との相互作用を熱力学的手法により調べたところ、RNAアプタマーに比べてキメラアプタマーでは、標的タンパク質との結合に伴うエンタルピー利得が大きい一方で、結合によって分子の自由度が失われることに由来するエントロピー損失(-TΔS)も大きいことが明らかになりました(図2)注3)。
そこで、NMRを用いて、アプタマー中の塩基対が開いたり閉じたりする動きを解析したところ、キメラアプタマーではRNAアプタマーよりも塩基対が開きやすく、分子の形が時間とともに変化する「ゆらぎ」が大きいことがわかりました。一本鎖のRNAは、さまざまな構造を形成して多くの生命現象に関わっています。一方で、DNAは二重らせん構造を形成して遺伝情報を保持しているため、RNAの方が自由度が高いと思われることがあります。しかし本研究では、RNAの一部をDNAに置き換えたキメラアプタマーの方が、RNAアプタマーよりも大きな「ゆらぎ」を示すことがわかりました。
さらに、コンピュータシミュレーションでも、キメラアプタマーは単独ではRNAアプタマーより大きく「ゆらぐ」一方、標的タンパク質に結合するとその動きが小さくなることが示されました。また、キメラアプタマーはRNAアプタマーよりも標的タンパク質の表面に広く接触し、よりよくフィットしていることが示されました。この結果は、キメラアプタマーで大きなエンタルピー利得が得られる理由を説明しています。これらの結果から、より柔らかいキメラアプタマーが標的タンパク質の表面に合わせて形を変えながら結合する、いわゆる誘導適合型の分子認識が起きていることが示されました。
<今後の展開>
本研究により、RNAとDNAを組み合わせることで、アプタマーの「ゆらぎ」や標的タンパク質へのフィットの仕方を変えられることが示されました。今後、この知見は、標的分子に合わせて結合特性を調整したアプタマー医薬品の開発に役立つと期待されます。
また、アプタマーセンサでは、金属イオンなどの条件を利用して標的分子への結合をオン・オフ制御する設計も可能です。この特徴を利用すれば、病気の診断だけでなく、日常的な健康状態のモニタリングや環境汚染物質の検出など、リアルタイムモニタリングに適したセンサの開発が期待されます。
RNA-DNAキメラアプタマーは、医療、診断、健康モニタリング、環境計測など幅広い分野で活用が期待される、次世代の核酸材料です。
<参考図>
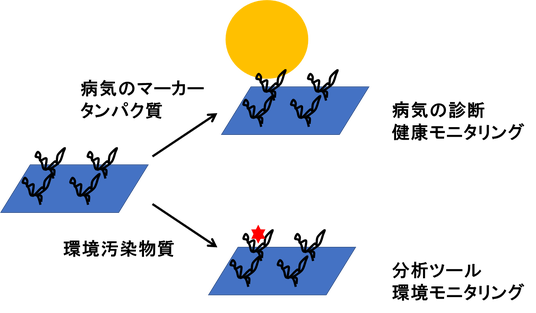
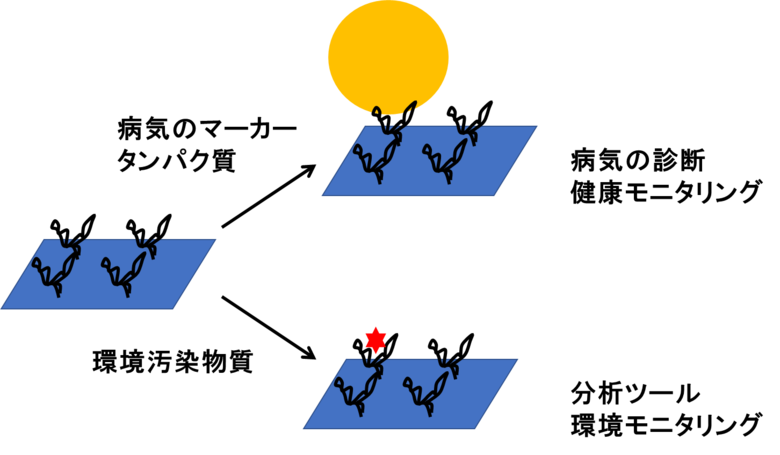
図1 バイオセンサ(アプタマーセンサ)のイメージ
アプタマーを基板上に固定化し、病気のマーカータンパク質や環境汚染物質などの標的分子を検出します。この仕組みは、病気の診断、健康モニタリング、分析ツール、環境モニタリングなどに応用できます。
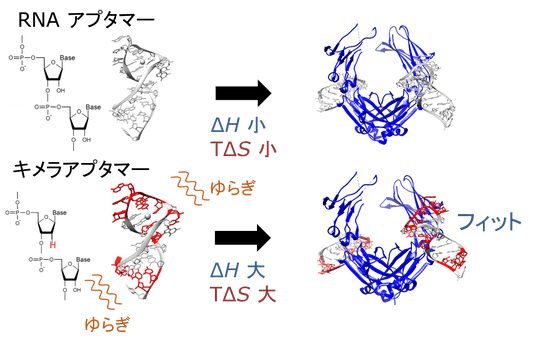
図2 RNAアプタマーとRNA-DNAキメラアプタマーの分子認識機構の違い
RNAアプタマーとRNA-DNAキメラアプタマーを比較したところ、キメラアプタマーでは分子の形が時間とともに変化する「ゆらぎ」が大きく、標的タンパク質との結合に伴って自由度が大きく低下することが示されました。一方で、柔らかいキメラアプタマーは標的タンパク質表面によりよくフィットし、大きなエンタルピー利得を示しました。その結果、キメラアプタマーではエンタルピー利得とエントロピー損失の両方が大きくなることが明らかになりました。
<論文情報>
論文題目:Impact of Nucleotide Flexibility on Aptamer−Protein Recognition: RNA vs RNA−DNA Chimera
(ヌクレオチドの柔軟性がアプタマー-タンパク質認識に及ぼす影響:RNAとRNA-DNAキメラの比較)
URL: https://pubs.acs.org/doi/10.1021/acschembio.6c00034
〈用語の説明〉
注1)核酸アプタマー
アプタマーは、「適合する」という意味からつくられた造語で、特徴的な立体構造を形成して標的分子に結合する人工的な核酸を指します。SELEX法によって得られるDNAまたはRNA分子で、標的タンパク質のはたらきを阻害、調節する医薬品候補として利用できるほか、標的分子を検出するバイオセンサ材料としても利用できます。
注2)SELEX法
SELEX (Systematic Evolution of Ligands by EXponential enrichment) 実験は、in vitro selection法ともよばれます。10¹⁵種類のランダムな配列の核酸プールを作成した後、その配列プールの中から標的分子に結合する配列の選別と増幅を繰り返すことで、標的分子に非常に強く特異的に結合するアプタマーを得ることができます。
注3)エンタルピー変化(ΔH)とエントロピー変化(ΔS)
物質の相互作用におけるエネルギー変化(ΔG)は、ΔG=ΔH-TΔSという熱力学の式で表すことができます。ΔHはエンタルピー変化で、水素結合、静電相互作用、ファンデルワールス相互作用などの形成に関係します。一方、ΔSはエントロピー変化で、分子の自由度や水和状態の変化に関係します。結合によって分子の動きが制限されると、エントロピー損失が生じ、−TΔSは結合を不利にする方向に働きます。本研究では、キメラアプタマーでエンタルピー利得が大きい一方、エントロピー損失も大きいことが示されました。
企業プレスリリース詳細へ
PR TIMESトップへ
データ提供 PR TIMES
本記事の内容に関するお問い合わせ、または掲載についてのお問い合わせは株式会社 PR TIMES (release_fujitv@prtimes.co.jp)までご連絡ください。また、製品・サービスなどに関するお問い合わせに関しましては、それぞれの発表企業・団体にご連絡ください。